
浙江大学脑科学与脑医学学院院长胡海岚教授,长期深耕情绪与社会行为的分子及神经环路机制领域,是2025年中科院院士增选有效候选人,这也是她第三次入围该候选名单。她带领团队在抑郁症发病机制、社会竞争神经基础等方向持续突破,发表多篇顶刊成果,近期更在Cell、Neuro等权威期刊连发最新研究。

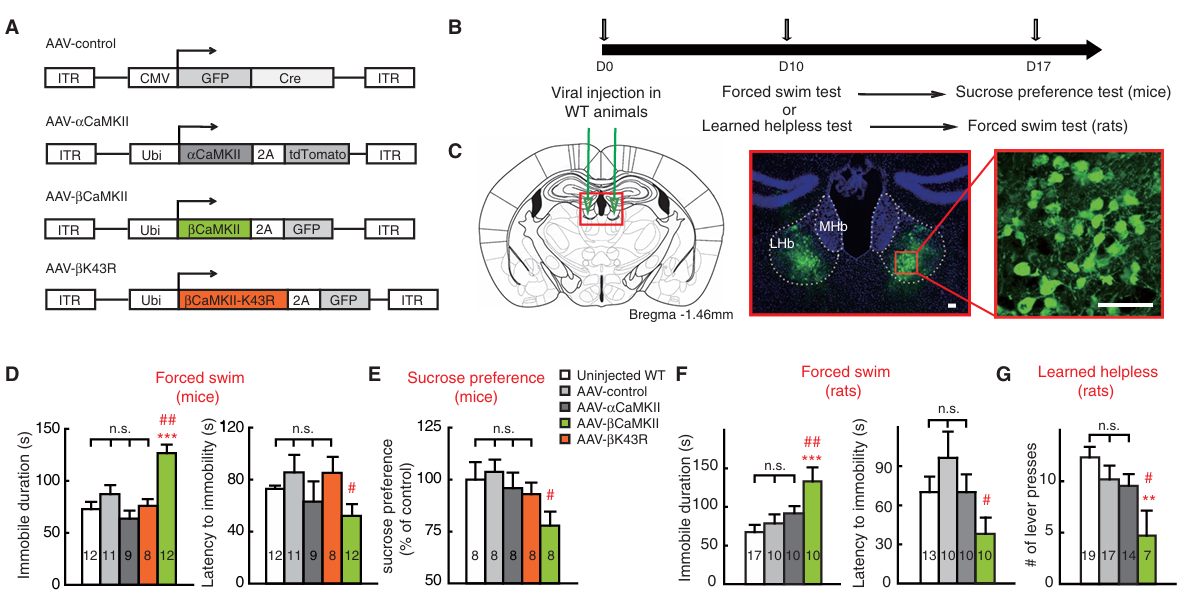
1. Science,论文题目βCaMKII in Lateral Habenula Mediates Core Symptoms of Depression,锁定抑郁核心调控分子,βCaMKII 成抗抑郁关键靶点
核心亮点:抑郁症的分子调控机制长期缺乏明确靶点,传统治疗手段效果有限。胡海岚团队发现,抑郁症动物模型的外侧缰核(LHb)中 βCaMKII 表达显著上调,且会被抗抑郁药反向调控。该分子可强效增强LHb神经元的突触效能和峰输出,单独升高其水平即能诱发严重抑郁症状;而下调其表达、阻断活性或抑制靶分子谷氨酸受体GluR1,可有效逆转抑郁症状。这一发现明确了βCaMKII作为LHb神经元功能调节因子和抑郁症关键决定因子的核心地位,为抗抑郁药物研发提供了精准分子靶点。
作者信息:胡海岚教授为通讯作者,浙江大学脑科学与脑医学学院团队为核心完成单位
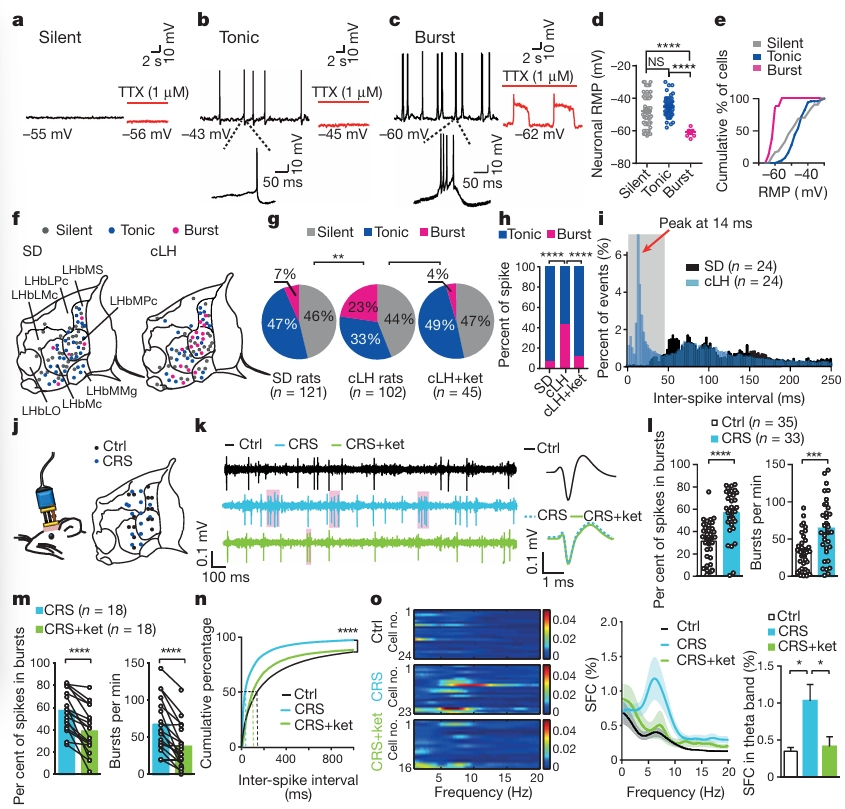
2. Nature,论文题目:Ketamine blocks bursting in the lateral habenula to rapidly relieve depression,破解氯胺酮快速抗抑郁之谜,簇状放电机制开辟新路径
核心亮点:传统抗抑郁药起效缓慢且应答率低,氯胺酮的快速抗抑郁效应缺乏明确机制解释。胡海岚团队首次发现,大脑 “反奖赏中心” 外侧缰核(LHb)的簇状放电是抑郁症发生的充分条件,这种特殊放电模式会强力抑制 “奖赏中心” 引发抑郁情绪。氯胺酮的核心作用是直接阻止LHb的簇状放电,快速解除其对 “奖赏中心” 的抑制,40分钟内即可改善抑郁症状。研究同时揭示 T 型钙通道(T-VSCC)可作为新型抗抑郁靶点,为开发快速起效的抗抑郁药物提供了关键理论支撑。
作者信息:胡海岚教授为通讯作者,浙江大学脑科学与脑医学学院团队为核心完成单位
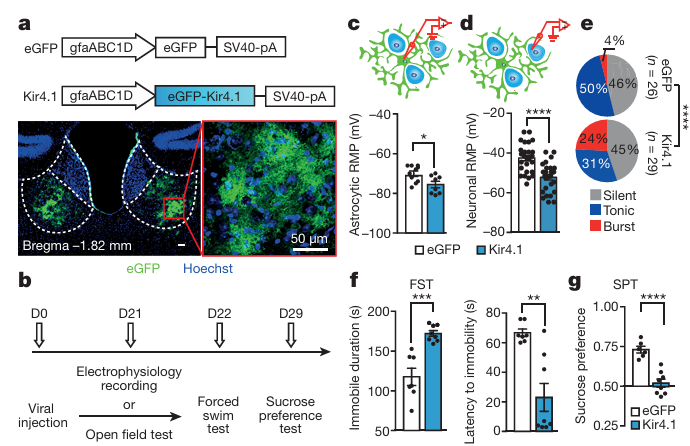
3. Nature,论文题目:Astroglial Kir4.1 in lateral habenula drives neuronal bursts in depression,揭示胶质细胞致抑郁机制,Kir4.1通道成干预新靶点
核心亮点:胶质细胞在抑郁症发病中的作用长期未被充分阐明,其与神经元的交互机制仍是研究空白。胡海岚团队聚焦外侧缰核(LHb),发现胶质细胞中的钾离子通道Kir4.1是诱发神经元超极化和簇状放电增加的关键分子。该通道的异常激活会直接驱动LHb神经元进入抑郁相关的簇状放电状态,是抑郁症发生的重要上游机制。这一发现首次明确了胶质细胞在抑郁发病中的核心作用,将Kir4.1通道确定为快速抗抑郁的全新靶点,丰富了抑郁症的多细胞调控理论。
作者信息:胡海岚教授为通讯作者,浙江大学脑科学与脑医学学院团队为核心完成单位
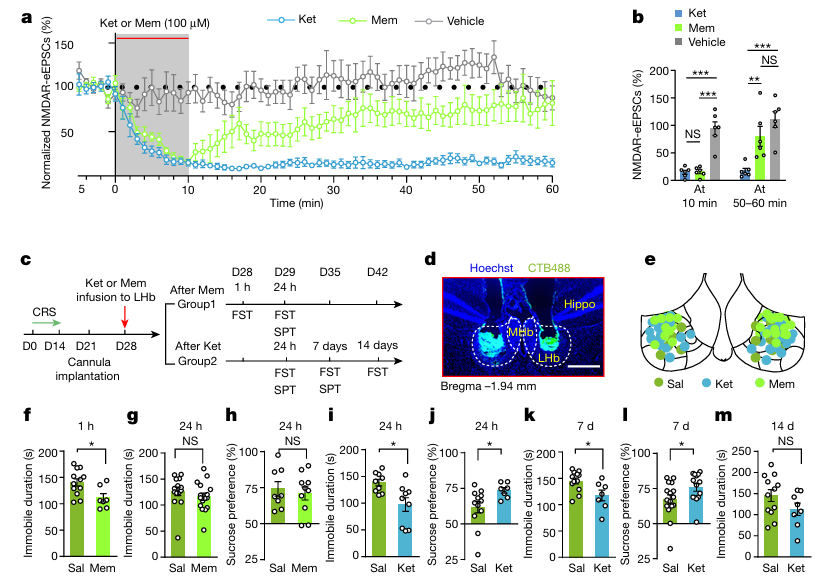
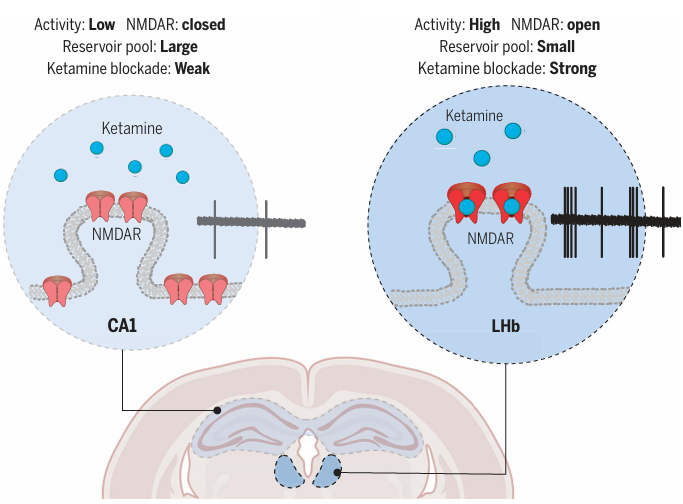
4. Nature,论文题目:Sustained antidepressant effect of ketamine through NMDAR trapping in the LHb,解析氯胺酮长效抗抑郁机制,NMDAR 滞留效应实现持久疗效
核心亮点:氯胺酮半衰期仅 13 分钟,但其抗抑郁效果却能持续一周,这种药代动力学与药效的巨大差异长期无法解释。胡海岚团队发现,氯胺酮作为 “陷入式阻断剂”,与外侧缰核(LHb)神经元的谷氨酸受体(NMDAR)结合后,会被 “滞留” 在受体通道内难以解离,从而躲开肝脏代谢酶的作用。即便 24 小时后血液中已检测不到药物,仍能持续阻断 LHb 簇状放电,维持抗抑郁效果。该研究揭示了氯胺酮长效作用的独特药化特征,为优化临床低剂量用药方案、设计长效抗抑郁药物提供了直接理论指导。
作者信息:胡海岚教授为通讯作者,核心完成单位包括浙江大学医学院脑科学与脑医学学院、教育部脑与脑机融合前沿科学中心、脑机智能全国重点实验室、良渚实验室,博士生马爽爽与博士后陈敏为共同第一作者
5. Science,论文题目:Brain region–specific action of ketamine as a rapid antidepressant,明确氯胺酮脑区特异性靶点,解析上下游信号通路关联
核心亮点:氯胺酮为何优先靶向外侧缰核(LHb)发挥抗抑郁作用,其脑区特异性机制及上下游信号传导路径尚未明确。胡海岚团队在前期研究基础上,进一步揭示了LHb成为氯胺酮首选靶向脑区的神经基础,首次清晰描述了从LHb到海马脑区的上下游信号通路关联。该成果完善了以外侧缰核 NMDAR 为核心的氯胺酮抗抑郁机制理论体系,为理解药物的脑区特异性作用提供了全新视角,也为临床用药策略优化和新型靶向药物研发提供了更精准的理论支持。
作者信息:胡海岚教授为通讯作者,浙江大学脑科学与脑医学学院团队为核心完成单位
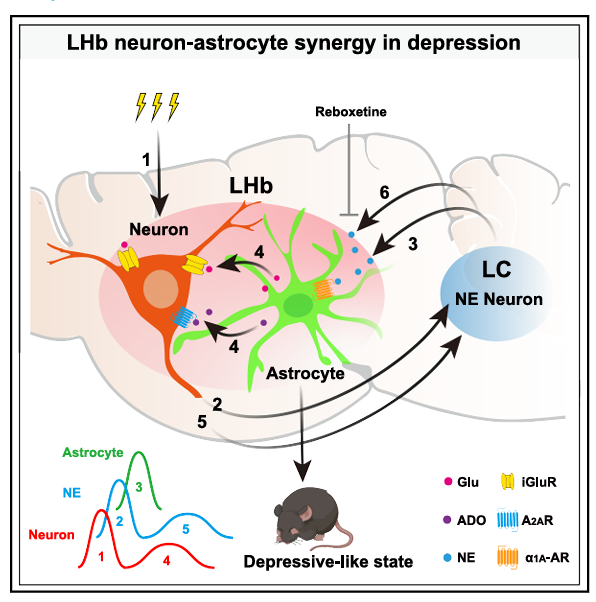
6. Cell,论文题目:Neuron-astrocyte Coupling in Lateral Habenula Mediates Depressive-like Behaviors,揭秘抑郁发生 “铁三角” 环路,细胞交互机制开辟防治新路径
核心亮点:抑郁症已成为全球高发精神障碍,但压力诱发抑郁的动态细胞交互机制尚未明确。胡海岚团队聚焦神经元与星形胶质细胞两大核心细胞类群,首次绘制出大脑压力信号传输时序图谱,发现外侧缰核(LHb)神经元、蓝斑核去甲肾上腺素能(LC-NE)神经元及 LHb 星形胶质细胞构成的循环 “铁三角” 神经网络。该环路的反复激活是抑郁发作的关键诱因,同时揭示出去甲肾上腺素(NE)对抑郁的调控核心在于 “释放节奏” 而非 “总量”。这一发现打破了传统单一细胞研究范式,为压力管理和抑郁症预防提供了全新诊疗靶点与策略。
作者信息:胡海岚教授为通讯作者,浙江大学脑科学与脑医学学院、双脑中心为核心完成单位,博士生辛倩倩、王俊盈为共同第一作者
7. Science,论文题目:Bidirectional Control of Social Hierarchy by Synaptic Efficacy in Medial Prefrontal Cortex,调控社会等级可塑性,前额叶皮层突触效能成核心开关
核心亮点:社会等级的神经调控机制及可塑性潜力长期不明确,缺乏直接干预靶点。胡海岚团队通过动物实验证实,小鼠社会地位等级相对稳定且具有传递性,与内侧前额叶皮层(mPFC)第V层锥体神经元的兴奋性突触输入强度高度相关 —— 等级越高的小鼠,突触输入强度越高。通过分子操作增强背内侧前额叶皮层(dmPFC)神经元突触效能,可提升动物社会等级;反之则导致等级下降。该研究首次为mPFC参与社会等级调控提供直接证据,证实社会等级的可塑性,为干预社会行为相关障碍提供了关键靶点。
作者信息:胡海岚教授为通讯作者,浙江大学脑科学与脑医学学院团队为核心完成单位
8. Science,论文题目:History of winning remodels thalamo-PFC circuit to reinforce social dominance,解码 “胜利者效应” 神经环路,丘脑 - 前额叶通路介导竞争优势
核心亮点:“胜利者效应”(既往胜利经历助力后续竞争获胜)是社会竞争的关键现象,但其潜在神经环路长期未知。胡海岚团队首次发现,哺乳动物大脑中 “中缝背侧丘脑投射到前额叶皮层” 的神经环路是介导该效应的核心。这一环路通过重塑神经连接,将既往胜利经历转化为后续竞争优势,让 “赢者更赢”。该研究建立了社会竞争优势形成的环路机制框架,为理解适应性与病理性社会行为提供了全新视角,也为相关社会行为障碍的干预提供了特异性靶点脑区。
作者信息:胡海岚教授为通讯作者,核心完成单位为浙江大学求是高等研究院系统神经与认知科学研究所和医学院神经科学研究中心,博士生周亭亭、朱鸿和范郑晓等为核心参与者
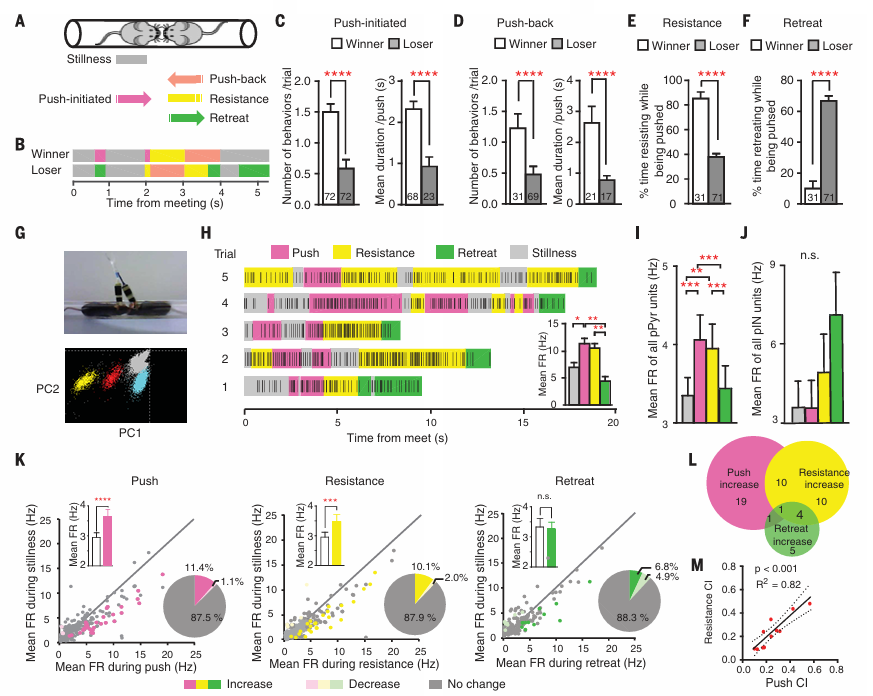
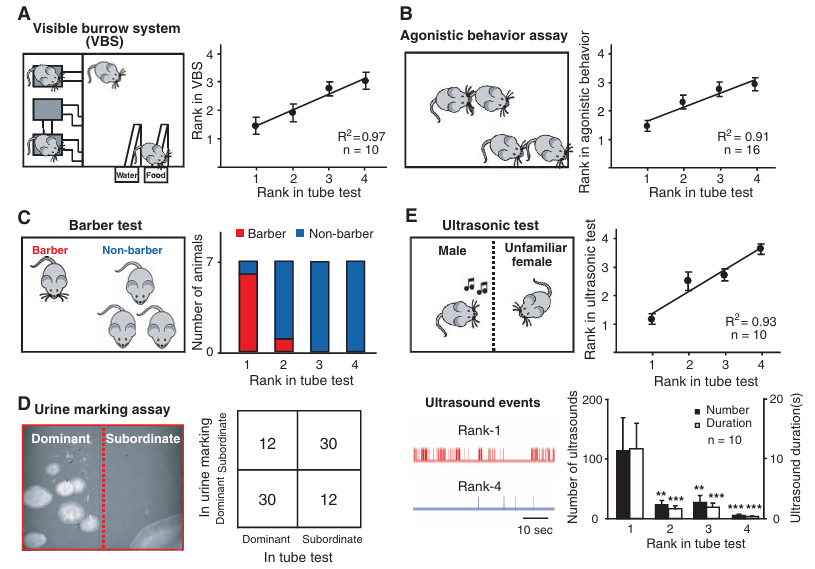
9. Cell,论文题目:Neural Mechanism Underlying Depressive-Like State Associated with Social Status Loss,揭示社会地位丧失致郁机制,建立竞争与情绪关联通路
核心亮点:社会地位下降是抑郁症的重要诱因,但两者间的神经关联机制尚未明确。胡海岚团队发现,社会地位下降会触发负性奖赏预测误差,进而激活大脑反奖赏中枢外侧缰核(LHb)。LHb的激活一方面直接诱导抑郁样行为,另一方面抑制负责调控社会竞争力的内侧前额叶皮层(mPFC),形成 “地位下降-抑郁-竞争能力减弱” 的恶性循环。研究同时证实,氯胺酮治疗可提升竞争失败小鼠的获胜概率和社会等级,而激活mPFC恢复社会地位能快速改善抑郁样行为,为社会因素诱发抑郁症的干预提供了双重理论依据。
作者信息:胡海岚教授为通讯作者,核心完成单位包含浙江大学脑科学与脑医学学院、教育部脑与脑机融合前沿科学中心、脑机智能全国重点实验室、良渚实验室,博士生范郑晓为第一作者,博士生常家瑞、梁艺蓝等做出重要贡献
胡海岚教授深耕情绪与社会行为的分子及神经环路机制研究,带领团队在抑郁症发病机制、社会竞争神经基础等领域取得重大突破。她的团队明确了βCaMKII、Kir4.1通道等多个抑郁症关键分子靶点,破解了氯胺酮快速及长效抗抑郁的核心机制,揭示了外侧缰核相关神经环路在抑郁发生中的关键作用,还阐明了社会等级调控及地位丧失致郁的神经机制。这些成果推动我国情绪神经科学跻身国际领先行列,为精神健康领域的精准治疗与防控提供了重要理论支撑和潜在干预路径。
胡海岚教授简介:
